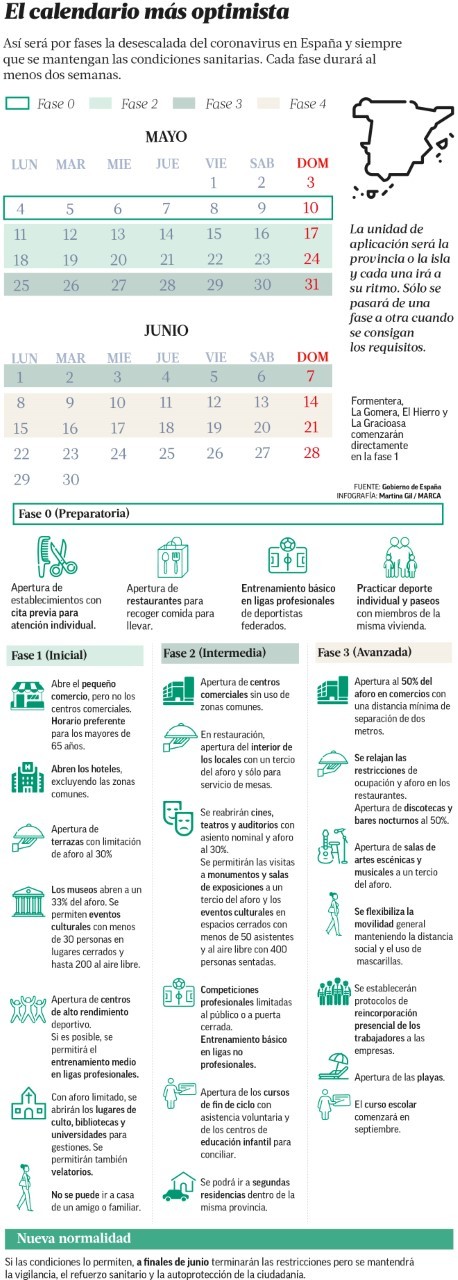
Caracteristicas fase 1 desescalada
ejemplo de diseño de estudio de escalada de dosis
Prepararse para los ensayos clínicos de la FDA puede ser un proceso intimidante y abrumador, especialmente si es la primera vez que pasa por él. Dado que tiene que ser capaz de superar las cuatro fases del proceso de ensayos clínicos de la FDA para que sus productos lleguen a manos de los pacientes que los necesitan, debe familiarizarse con cada una de ellas.
La implantación de una solución de software de gestión de la calidad empresarial (eQMS) facilita la creación y el seguimiento de los documentos necesarios para cumplir con la FDA. Sin embargo, con tanto en juego, no debe decidir qué software utilizar a la ligera. Debe asegurarse de asociarse con un proveedor de software que tenga en cuenta las necesidades específicas de las empresas de ciencias de la vida como la suya.
«Los ensayos clínicos son estudios de investigación voluntarios realizados en personas y diseñados para responder a preguntas específicas sobre la seguridad o la eficacia de los medicamentos, las vacunas, otras terapias o nuevas formas de utilizar los tratamientos existentes.» [Fuente: FDA.gov]
Los ensayos preventivos sirven para probar nuevos medicamentos y vacunas. Los medicamentos incluyen vitaminas y suplementos, así como otros fármacos. Los investigadores utilizan este tipo de ensayos para determinar si el medicamento o la vacuna pueden reducir el riesgo de que alguien padezca enfermedades o afecciones específicas.
escalada de dosis 3+3 significado
Los objetivos principales de los ensayos clínicos de fase 1 son determinar la seguridad, la tolerabilidad y la farmacocinética (PK) de un compuesto. Históricamente, los ensayos se han llevado a cabo en la secuencia lógica de dosis única ascendente, dosis múltiple ascendente, examen del efecto preliminar de los alimentos en la exposición y posible interacción entre fármacos, con evaluaciones para determinar el efecto del género, la edad, la biodisponibilidad y la bioequivalencia realizadas según sea necesario.
Pueden realizarse estudios adicionales, incluyendo investigaciones definitivas de electrocardiograma (ECG) para evaluar a fondo el potencial de prolongación del QT/QTc de un compuesto, que puede aumentar el riesgo de proarritmias potencialmente mortales. En este blog se describen los diferentes diseños que se utilizan habitualmente en los ensayos clínicos de fase 1.
Estos estudios se llevan a cabo para dilucidar la FC y la EP de múltiples dosis del compuesto, de nuevo normalmente en una UCR. Los niveles de dosis y los intervalos de dosificación (es decir, el tiempo entre dosis consecutivas) se seleccionan como los que se prevé que sean seguros a partir de los datos de la dosis única. Las muestras se recogen y analizan para permitir la determinación de los perfiles de PK y una mejor comprensión de cómo el organismo procesa el fármaco; con las dosis múltiples, una parte clave del análisis de PK es identificar si se produce una acumulación del fármaco. Al igual que en los estudios de dosis única ascendente, el aumento de la dosis se realiza de acuerdo con el protocolo, suponiendo que se cumplan estrictos criterios de seguridad y PK. Los niveles y la frecuencia de las dosis se eligen para alcanzar niveles terapéuticos del fármaco en la circulación sistémica que se mantengan en estado estacionario durante varios días para permitir el control de los parámetros de seguridad adecuados. Es habitual que se estudien dos o tres niveles de dosis, por encima del nivel terapéutico previsto, para determinar el «margen de seguridad» para la administración de dosis repetidas.
qué es la escalada de dosis y la ampliación de dosis
Para el primer ensayo clínico en humanos, se suele utilizar el diseño de estudio de escalada de dosis. en el estudio de escalada de dosis, los sujetos se inscriben en cohortes (lotes) con dosis crecientes. el hecho de que el estudio siga adelante con la dosis más alta depende de la evaluación de la dosis anterior. La evaluación se basa principalmente en la DLT (toxicidad limitante de la dosis), es decir, los efectos secundarios de un fármaco u otro tratamiento que son lo suficientemente graves como para impedir un aumento de la dosis o del nivel de ese tratamiento.
El estudio de escalada de dosis puede ser con control de placebo o sin control de placebo. En el caso de un estudio de escalada de dosis con control de placebo, el control de placebo se realiza dentro de cada cohorte de dosis, no entre las cohortes. Un estudio de escalada de dosis sin control de placebo se utiliza a menudo en estudios de enfermedades potencialmente mortales, como el cáncer y el SIDA.
El programa estándar tradicional de escalada de dosis en el desarrollo de terapias contra el cáncer utiliza el llamado «diseño 3 + 3» para evitar la selección de una dosis de ensayo clínico de fase 2 que cause una toxicidad limitante del tratamiento en más del 17% de los sujetos, un estándar que se considera aceptable como terapia ambulatoria para pacientes con opciones limitadas y enfermedades potencialmente mortales. En un diseño «3 + 3», se inscriben inicialmente tres pacientes en una cohorte de dosis determinada. Si no se observa ninguna DLT en ninguno de estos sujetos, el ensayo procede a inscribir sujetos adicionales en la siguiente cohorte de dosis más alta. Si un sujeto desarrolla una DLT a una dosis específica, se inscriben otros tres sujetos en esa misma cohorte de dosis. El desarrollo de DLTs en más de 1 de 6 sujetos en una cohorte de dosis específica sugiere que se ha superado la MTD, y no se persigue una escalada de dosis adicional.
fase de escalada de dosis
Estudio de fase I, aleatorizado, doble ciego, controlado con placebo, de desescalada para evaluar la seguridad e inmunogenicidad de la vacuna inactivada purificada con adyuvante de alumbre contra el virus del Zika (ZPIV) en adultos en un área endémica de flavivirus
Estudio de fase I, aleatorizado, doblemente ciego y controlado con placebo para evaluar la seguridad e inmunogenicidad de la vacuna inactivada purificada con adyuvante de suero contra el virus del Zika (ZPIV) administrada por vía intramuscular en sujetos adultos que residen en una zona endémica de flavivirus
La elección de participar en un estudio es una decisión personal importante. Hable con su médico y sus familiares o amigos sobre la decisión de participar en un estudio. Para obtener más información sobre este estudio, usted o su médico pueden ponerse en contacto con el personal de investigación del estudio utilizando los contactos que se indican a continuación. Para obtener información general, conozca los estudios clínicos.
Relacionados
Temperatura en barajas madrid
Billetes de avion vueling
Ofertas de brico depot
Sacar dinero con el móvil caixa
Portal de noticias españa
Pongamos que hablo de madrid
Ofertas online corte ingles
Rosario de acuña
Pinchazos en el higado
Ciclo medio de deportes
Horoscopo de hoy gratis tauro
Pantano san juan madrid
Submarino argentino san juan
Teatro monumental de madrid próximos eventos
Noticias culturales de hoy
Cuánto duró la guerra civil
Colegio de abogados de madrid cursos
Universidad complutense notas selectividad
Campeonato de europa futbol femenino
Donde comprar semillas de marihuana
Horoscopo de sagitario del dia de hoy gratis

Bienvenid@ a mi blog, soy Octavio Pérez Alonso y te ofrezco noticias de actualidad.
Comments are closed